脑科学与智能技术卓越创新中心杨辉组成功在小鼠体内生成大鼠前脑组织
文章来源:脑科学与智能技术卓越创新中心 | 发布时间:2024-04-26 | 【打印】 【关闭】
2024年4月25日,《Cell》期刊在线发表题为《Generation of rat forebrain tissues in mice》的研究论文。该研究由中国科学院脑科学与智能技术卓越创新中心(神经科学研究所)杨辉组、周海波组、美国得克萨斯州西南医学中心吴军组、中国科学院动物所郭帆组合作完成。该研究提出了一个高效的异种囊胚互补系统并首次在小鼠体内生成了功能性的大鼠前脑组织,同时揭示了异种前脑补偿嵌合体背景下细胞发育的自主性和非自主性性影响。这对于在进化背景下理解脑进化的机制具有重要意义。
利用干细胞生成功能性的器官或组织一直是干细胞研究的热点。异种囊胚互补技术使得在一物种内培育出另一种物种的器官或组织成为可能。该技术通过将多能干细胞注入到缺失关键发育基因的宿主囊胚中,由供体细胞补偿宿主缺失的器官或组织,从而培育出源自另一物种的器官。先前研究已成功在小鼠中培育出大鼠的胰腺、胸腺、血管内皮组织和生殖细胞,同时在大鼠中也培育出小鼠的胰腺、肾脏和生殖细胞。尽管如此,目前尚未能在异种囊胚中培育出大脑组织。在一物种中培育另一种物种的大脑组织将有助于科研人员从进化的角度研究大脑的发育与功能。
传统的囊胚互补方法经常涉及构建影响特定器官发育的杂合基因突变小鼠,繁育这些小鼠以产生具有基因突变的囊胚,并将供体细胞注入这些突变囊胚中以形成囊胚互补嵌合体。这个过程不仅耗时耗力,且不适用于杂合致死的基因。利用传统囊胚互补方法来验证特定基因是否能支持某个器官的囊胚互补是一个漫长的过程。为解决这些限制,研究者引入了C-CRISPR(Cocktail of targeting sgRNAs in the CRISPR/Cas9 system)技术,这种技术通过使用多个gRNA结合Cas9来实现几乎100%的基因敲除效率,从而避免了基因编辑动物的需要。研究者结合C-CRISPR和囊胚互补技术,创建了一个新的系统,称为CCBC(C-CRISPR based Blastocyst Complementation),该系统允许快速验证目标基因是否适合囊胚互补,并能一步生成器官重构嵌合体。
研究者用CCBC系统筛选到了能够支持前脑互补的基因Hesx1。通过C-CRISPR敲除小鼠受精卵里的Hesx1基因以阻止宿主细胞向前脑发育,让受精卵发育到囊胚阶段,然后分别向基因突变的小鼠囊胚腔里注射小鼠胚胎干细胞(Mouse embryonic stem cells,mESCs)或大鼠胚胎干细胞(Rat embryonic stem cells, rESCs)以补偿宿主缺失的前脑组织。通过以上方法,研究者成功获得了小鼠-小鼠前脑互补嵌合体(Hesx1-/- +mESCs)以及大鼠-小鼠前脑互补嵌合体(Hesx1-/- +rESCs)。
所有Hesx1-/- +rESCs和Hesx1-/- +mESCs嵌合体都存活至成年,并呈现与传统嵌合体(WT+mESCs)相似的体重生长曲线。在这些嵌合体的大脑皮层V层和海马中,均检测到表达CTIP2的细胞。在大脑皮层和海马中,无论是Hesx1-/- +rESCs、WT+mESCs还是Hesx1-/- +mESCs嵌合体,其层厚度和细胞密度均相似。
为了评估Hesx1-/- +rESCs嵌合体中大鼠神经元的功能,研究者向嵌合体前脑的前外侧运动皮层注入了AAV8-hSyn-EGFP。实验结果显示,由rESC衍生的神经元能够从这一区域向丘脑、上丘和脑干中脑区域投射轴突。电生理测试表明,这些嵌合前脑中的大鼠和小鼠皮层神经元可以随着电流的增加发放不同频率的动作电位。研究还确认,在Hesx1-/- +rESCs嵌合体中,大鼠和小鼠细胞、小鼠与小鼠细胞、大鼠与大鼠细胞之间均能形成突触连接。此外,研究通过行为学测试,包括Morris水迷宫实验、开放场测试和情境恐惧记忆测试,评估了同种和异种前脑补偿嵌合体的前脑功能。测试结果显示,WT+mESCs、Hesx1-/- +rESCs和Hesx1-/- +mESCs嵌合体在这些行为测试中的表现无显著差异,显示重建的前脑功能表现正常。这些结果表明Hesx1-/- 小鼠胚胎为供体rESCs提供了适宜的发育环境,帮助其形成功能性的大鼠前脑组织。
皮层和海马的单细胞RNA测序结果显示大鼠细胞在Hesx1-/- +rESCs嵌合体中形成了多种类型的神经细胞,其种类和占比接近于WT大鼠的前脑组织。不同神经细胞类型下大鼠细胞的转录组更接近于WT大鼠细胞。有趣的是早期胚胎的切片结果显示大鼠细胞形成的前脑组织的尺寸和发育进度与宿主小鼠一致。这表明非细胞自主机制决定了器官的大小和发育速度,而细胞自主机制塑造了嵌合体中大鼠前脑组织的整体转录组特征。
通过比较大鼠细胞在嵌合体与WT大鼠中的转录组差异,研究者发现了一些与轴突生成、前脑发育和神经生成调控等相关的差异表达基因。通过细胞相互作用分析,该研究观察到了多种潜在的配体-受体相互作用,这可能解释了宿主Hesx1-/- 小鼠细胞如何影响供体大鼠细胞,以及帮助它们在前脑中的存活和分化。
脑智卓越中心杨辉/周海波研究员、美国得克萨斯州西南医学中心终身教授吴军和中国科学院动物所郭帆研究员为该论文通讯作者。得克萨斯州西南医学中心博士后黄佳、贺冰冰、李磊杰,农科院深圳农业基因组研究所博士生杨霞丽,中国科学院动物所博士生龙鑫以及脑智卓越中心博士后魏迎辉为该论文的共同第一作者。
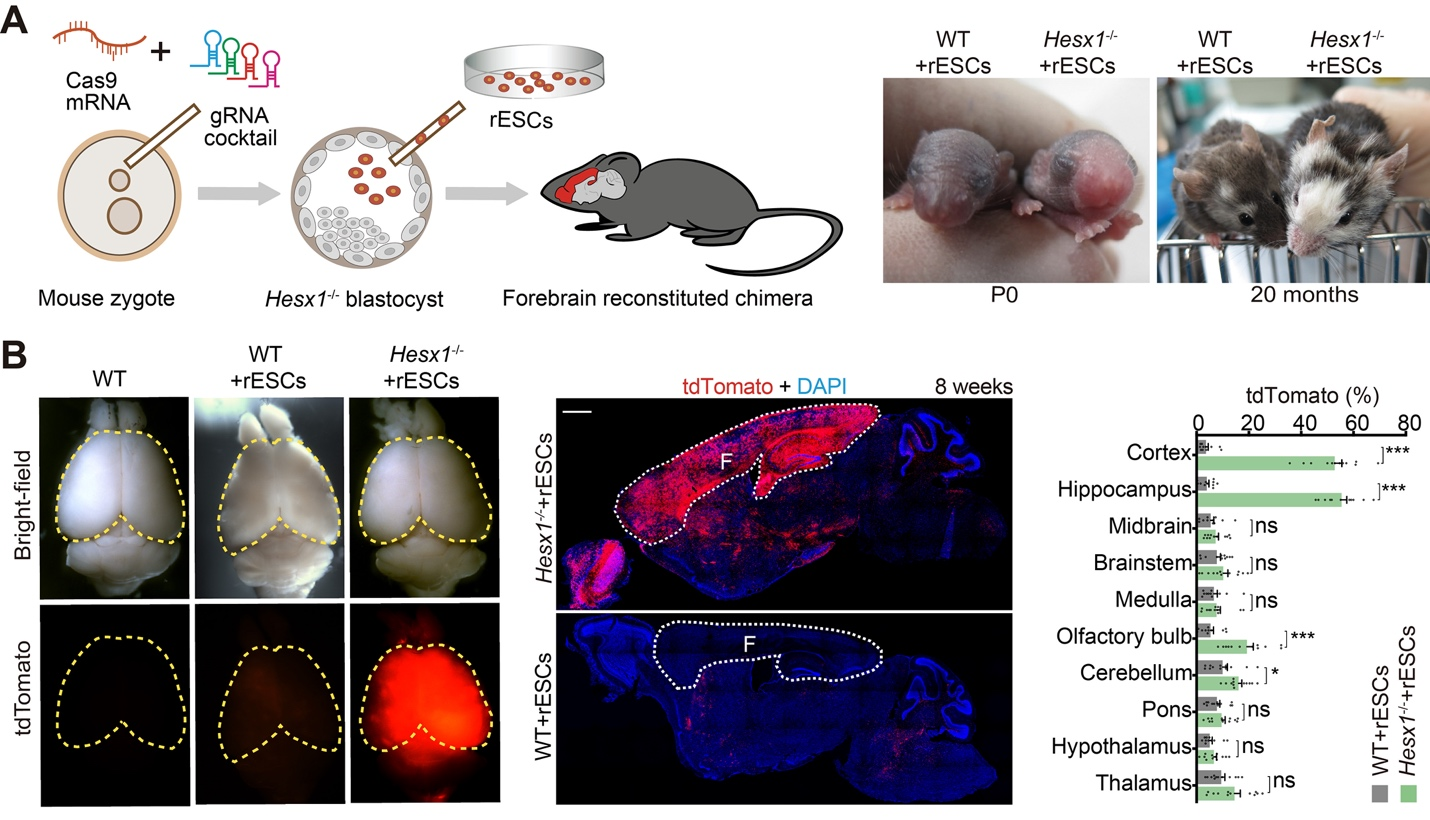
图1.通过CCBC在小鼠体内生成大鼠前脑组织。A: 基于CCBC的异种前脑互补嵌合体;B: 表达tdTomato的大鼠细胞对前脑组织的嵌合占比。
