2024年9月2日,中国科学院上海药物研究所张翾课题组与中国科学院昆明动物所何永捍课题组合作在Journal of Controlled Release发表了题为“Liver-targeting chimeras as a potential modality for the treatment of liver diseases”的最新研究成果。研究团队开发了一类能特异靶向肝脏蛋白的降解剂(Liver-Targeting Chimera, LIVTAC),成功实现了肝内靶蛋白的精准降解,并在肝细胞癌(hepatic cell carcinoma, HCC)模型上进行了概念验证。
肝癌是我国发病率排名第四、死亡率位居第二的恶性肿瘤,其中HCC是最常见的肝癌类型。大多数患者确诊时已是癌症晚期,几乎无法治愈。现有的肝癌治疗药物面临靶标稀缺、副作用大、治疗应答率低及容易产生耐药等诸多挑战。BET蛋白家族与肝癌的进展密切相关,多种BET抑制剂已进入临床试验,但研究发现BET抑制剂存在以血小板毒性为代表的“在靶毒性”,极大限制了该类药物的疗效与安全性。近年来,蛋白靶向降解嵌合体(Proteolysis-targeting chimera, PROTAC)技术凭借其独特的催化降解机制,能够有效提升药效。然而,PROTAC存在组织靶向性不足、成药性优化困难以及水溶性差等难题,一直难以攻克。
为此,研究团队利用肝实质细胞特异高表达去唾液酸糖蛋白受体(ASGPR)的特点,将PROTAC分子和ASGPR配体相偶联,借此实现PROTAC的肝脏靶向摄取和释放。代表性LIVTAC分子XZ1606表现出优异的蛋白降解能力和体外抗癌活性。机制研究表明,XZ1606与ASGPR结合后以内吞的方式被摄取,在细胞溶酶体被组织蛋白酶B剪切后释放出PROTAC分子,进而通过泛素-蛋白酶体途径对靶蛋白实施有效降解,最终促进肝癌细胞的凋亡和生长抑制(图1)。XZ1606在小鼠肝癌移植瘤模型中展现出良好的抗肿瘤活性。研究团队进一步将XZ1606与索拉非尼联合使用,发现联合用药能更有效地抑制肝癌细胞异体移植瘤的生长,显著延长荷瘤小鼠的总生存期,最重要的是在药效提升的同时未观察到明显的血小板毒性。以上结果证明,LIVTAC作为一种新型的HCC治疗手段,可有效避免传统药物干预手段因分子靶向性不足而产生的“在靶毒性”,突显了其转化应用的巨大潜力,有望用于其它肝脏疾病的治疗。
上海药物所硕士研究生陈川杰(现留所工作)和昆明动物所博士研究生潘永涨为本论文的共同第一作者,上海药物所张翾研究员和昆明动物所何永捍研究员为论文的共同通讯作者。该工作得到了国家自然科学基金、云南省基础研究计划、国家重点研发计划“主动健康和人口老龄化科技应对”重点专项及中国科学院率先行动“引才计划”等项目的资助。
全文链接:https://doi.org/10.1016/j.jconrel.2024.08.044
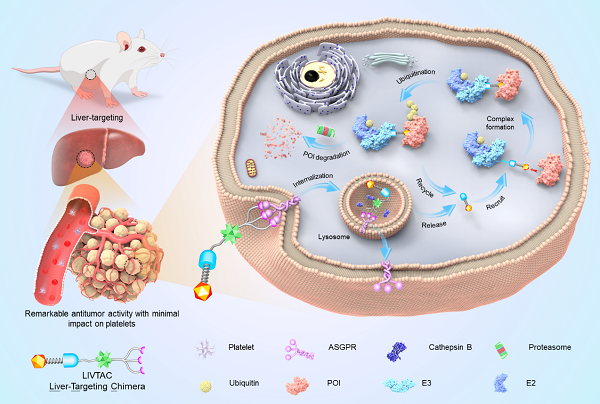
图1. LIVTAC分子作用原理示意图
(供稿部门:张翾课题组)

