2024年12月4日,上海药物所李亚平团队、上海科技大学张鹏程团队联合在Advanced Science上发表了题为“Interleukin 15-Presenting Nanovesicles with Doxorubicin-Loaded Ferritin Cores for Cancer Immunochemotherapy”的研究论文。该研究构建了一种酸敏感表面高表达膜结合形式IL15c的包载阿霉素铁蛋白内核的囊泡(DoxFILN),通过配体-受体识别分别靶向并作用于免疫细胞和肿瘤细胞,将免疫因子疗法与化疗结合,诱导强效的免疫杀伤。
白细胞介素15(IL15)对于促进自然杀伤(NK)细胞和细胞毒性T淋巴细胞(CTL)的存活和增殖至关重要。然而,IL15补充疗法仍面临诸如全身炎症和癌细胞非特异性刺激等挑战。此外,如何在引发肿瘤细胞免疫原性死亡(ICD)的同时,降低对瘤内免疫细胞的损伤也是亟待解决的问题。
为此,研究团队设计了一种pH响应性穿膜肽M70(pH-M70)修饰的纳米囊泡,该纳米囊泡由IL15c呈递膜和载有阿霉素的铁蛋白(Dox-Fn)核心组成(DoxFILN)。在肿瘤微酸环境中,穿膜肽M70激活,破坏DoxFILN,从而释放Dox-Fn和膜结合IL15c。Dox-Fn靶向癌细胞上的转铁蛋白受体1(TfR1)以诱导ICD,膜结合IL15c识别IL-15Rβ/γc,促进CTL和NK细胞的增殖和活化。在原位三阴性乳腺癌(TNBC)小鼠模型上证明了DoxFILN增加了CTL和NK细胞的募集、增殖和活性,最终产生显著的抗肿瘤功效。
上海药物所李亚平研究员、上海科技大学张鹏程研究员、上海药物所博士后蔡颖为本文的共同通讯作者,上海药物所博士生翟艺慧、硕士生张文为本文共同第一作者。该研究得到了国家重点研发计划、国家自然科学基金、山东实验室等项目的资助。
全文链接:https://doi.org/10.1002/advs.202409194
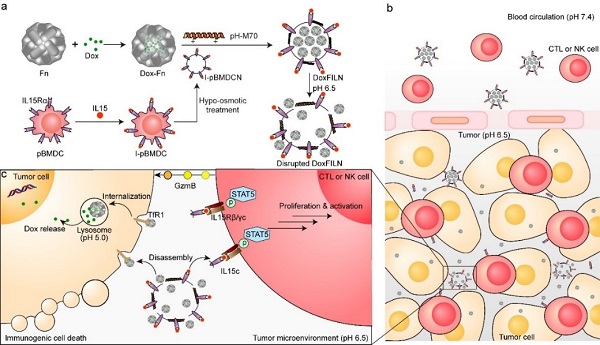
DoxFILN的制备和作用机制
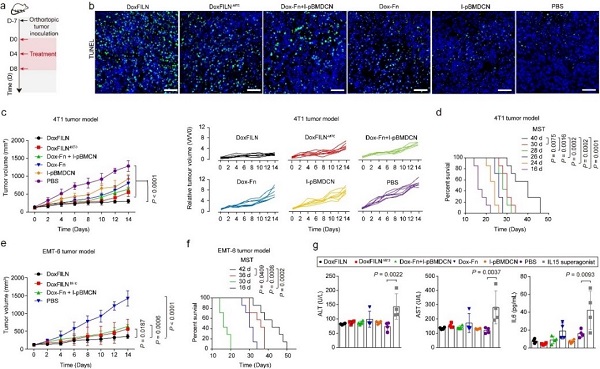
DoxFILN的抗TNBC效果
(供稿人:药物制剂研究中心;供稿人:蔡颖)

