2024年12月29日,中国科学院上海营养与健康研究所Andrew Teschendorff研究组在学术期刊Aging发表了题为“Cell-type specific epigenetic clocks to quantify biological age at cell-type resolution”的封面文章。该研究利用表观遗传时钟量化单一细胞类型的生物衰老,并为构建更有意义的分子时钟指引了方向。
表观遗传时钟是用于测量实际年龄和生物年龄的一种机器学习预测器,在许多科研领域得到广泛应用,可用于监测健康衰老或检验抗衰老干预措施在人体和动物模型中的功效。然而,表观遗传时钟的构建和解读的一大挑战,是复杂组织中潜在的细胞类型异质性,因为这些组织的细胞类型组成会随着年龄发生变化。当前的表观遗传时钟是由两个过程组成的复合体:一个“外在”过程捕捉细胞类型组成的年龄相关变化,另一个“内在”过程捕捉发生在单个细胞类型中的年龄相关表观遗传(DNA 甲基化)变化。目前尚不清楚表观遗传时钟的准确性,有多少归因于这些不同的外在和内在衰老过程。此外,如何将“内在”过程量化为单个细胞类型的衰老过程也尚不清楚。因此,有待提出一种在细胞类型分辨率上量化生物衰老的方法。
研究团队利用大量的血液和脑组织 DNA 甲基化数据集,展示表观遗传时钟在血液中高达 39%的准确性是受naïve T细胞和其他免疫细胞比例的潜在变化所驱动。而在脑组织中,这一“外在”过程的占比要低得多(12%),主要由神经元亚群的变化所驱动。Andrew Teschendorff研究员表示:“人们很长时间以来一直知道血液的衰老与naïve T细胞比例的变化有关,我们的工作现已量化了这种外在过程对表观遗传时钟准确性的贡献。这些贡献,目前只是下限,随着我们逐渐掌握更好的方法,以更高的细胞分辨率量化细胞类型比例,这个贡献值可能会上升。”
研究团队开发了一种在细胞类型分辨率上量化生物衰老的统计方法,构建了两种组织类型(大脑和肝脏)的细胞类型特异性 DNA 甲基化时钟,证明了与Horvath钟等泛组织钟相比,神经元和肝细胞特异性时钟在纯化的神经元和肝细胞中能更准确地预测实际年龄。与组织特异性或泛组织时钟相比,这些细胞类型特异性表观遗传时钟能更好地估计生物年龄。研究团队发现胶质细胞特异性时钟在阿尔茨海默病患者的颞叶中显示出特别显著的年龄加速,这强化了胶质细胞中的表观遗传学变化可能是神经退行性疾病的重要影响因素的观点。与之一致的是,近期发表的DamAge 时钟,其CpG 可能与促进不良健康结果有因果关系,研究团队的神经元和胶质细胞特异性时钟中, CpG 与构成 DamAge 时钟的 CpG 显著重叠。正如文章通讯作者Andrew Teschendorff所说:“神经元和胶质细胞特异性时钟中的 CpG ,能被关联到已被证实与神经退行性疾病有因果关系的基因,表明我们正在朝着构建更有意义的分子时钟的正确方向迈进。”接下来,研究团队将进一步探索年龄相关表观遗传变化与神经退行性疾病之间的因果关系。
中国科学院上海营养与健康研究所博士生童惠格和郭晓龙为文章的共同第一作者,Andrew Teschendorff研究员为通讯作者。该工作获得国家自然科学基金委员会和中国科学院的资助。文中分析的数据集来自公开数据库。
原文链接:https://doi.org/10.18632/aging.206184
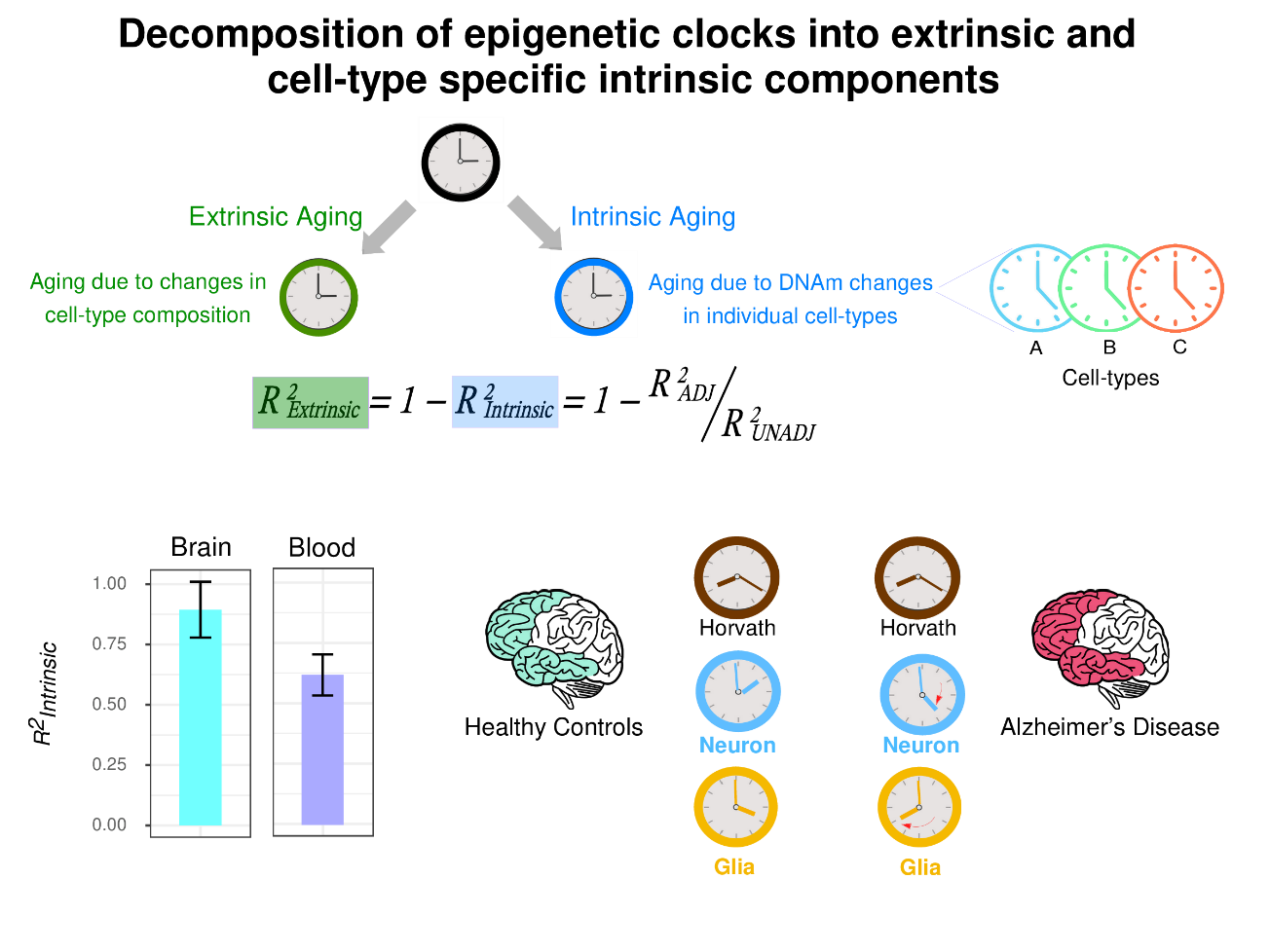
图:表观遗传时钟是一个复合物,它反映了两种衰老过程,一个是细胞组成与年龄相关的变化(“外在的”),另一个是单一细胞类型内与年龄相关的DNA甲基化变化(“内在的”)。这些变化可能在不同细胞类型之间有所不同,因此构建特定细胞类型的表观遗传时钟至关重要。研究团队对大脑和血液中衰老的内在过程进行了量化。在血液中,外在过程的影响要大得多,这是由于免疫细胞组成与年龄变化显著相关。通过比较阿尔茨海默病患者前额叶和颞叶的表观遗传时钟估计值与对照组的估计值,研究团队发现在阿尔茨海默病患者中,胶质细胞和神经元时钟会发生加速,而Horvath和其他非细胞类型特异的时钟则没有发生加速,胶质细胞时钟在阿尔茨海默病患者中显示出最显著的年龄加速。

