分子细胞科学卓越创新中心周斌组揭示心脏损伤修复中冠状动脉的新来源及形成过程
文章来源:分子细胞科学卓越创新中心 | 发布时间:2022-05-02 | 【打印】 【关闭】
4月11日,国际学术期刊Circulation 在线发表了中国科学院分子细胞科学卓越创新中心周斌研究组题为“Dual Genetic Lineage Tracing Reveals Capillary to Artery Formation in the Adult Heart”的最新研究成果。该研究利用双同源重组酶介导的遗传谱系示踪技术高效且清晰地记录成体心脏损伤过程中毛细血管形成冠状动脉的过程,揭示了毛细血管动脉化在成体心肌缺血模型中的重要作用,为受损心脏的血管修复和治疗提供了新的研究方向,为心血管再生医学提供了新思路。
冠状动脉疾病一直是全人类致死率最高的疾病之一。冠状动脉一旦发生病变,将阻碍血液有效流向心肌,导致心肌组织缺乏必需的氧气和营养物质,从而引发心肌梗死。如何使病变的冠状动脉再度发挥血流作用(血运重建)或者刺激新的冠状动脉生成一直是该领域研究者努力的方向。支架植入和冠状动脉旁路移植技术的开发与发展使得血运重建成为可能,挽救了部分患者的生命。侧支动脉的形成为新生期梗死的心脏提供血流,从而缓解心脏衰竭。然而,有一定数量的患者由于身体原因不能接受血运重建的治疗,而侧支动脉的形成目前仍受限于新生期。因此,深入探究新生冠状动脉来源及形成机制将为心脏损伤后血管的修复与再生提供新的策略或方法。
目前,关于侧支动脉新生有两种解释模型。一种是动脉发生(Arteriogenesis),即预先存在的动脉通过快速的管腔开放和血管壁增厚产生侧支动脉(Helisch A et al.,Microcirculation 2003);另一种是动脉化(Arterialization),即毛细血管通过血管生成进行血管重塑,并招募周细胞和平滑肌细胞,以产生侧支动脉(Faber JE et al.,Arterioscler Thromb Vasc Biol 2014)。鉴于在成体心肌梗死过程中很少观察到毛细血管通过动脉化产生冠状动脉(He et al.,Cardiovasc Res 2016),目前的主流观点更偏向于用动脉发生模型解释新生的冠状动脉。然而,随着技术的发展,冠状动脉新生的方式仍需进一步研究。
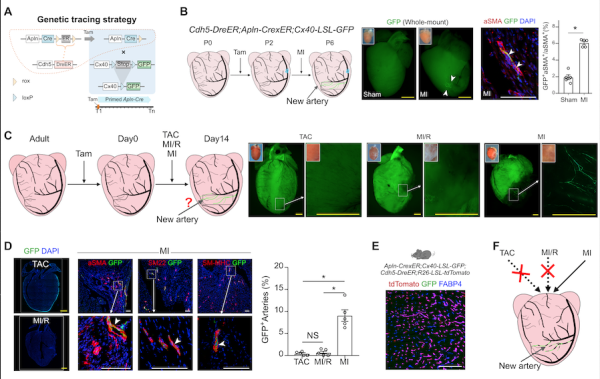
为灵敏且干净地检测到从毛细血管衍生出的动脉,研究人员在双同源重组酶介导的谱系示踪技术(He et al., Nature Medicine 2017)的基础上,建立了无缝隙捕捉毛细血管动脉化的新系统。前人的研究之所以很难在成体捕捉到毛细血管动脉化的过程,有以下两层阻碍。首先,毛细血管的分子标志物——Apln在成体心脏中只活跃于部分血管新生的毛细血管而非动脉内皮细胞,这就使得在成体心脏中高效地标记毛细血管内皮细胞成为一个技术难题。其次,若单纯标记毛细血管,想要在无数的毛细血管中找出由毛细血管动脉化产生的少量动脉无异于大海捞针,这种低分辨率的方法很容易让研究者忽视掉由毛细血管动脉化产生的动脉。为克服以上阻碍,周斌组研究人员利用Cdh5-DreER, Apln-CrexER和Cx40-LSL-GFP 三个小鼠品系,建立了一个在小鼠心脏中只标记由毛细血管衍生而来的动脉的系统。Cdh5-DreER是内皮特异性的小鼠品系,Apln-CrexER是毛细血管特异性的小鼠品系。Cx40-LSL-GFP可将动脉标记成绿色。当受到他莫昔芬的诱导后,Cdh5-DreER的DreER便会入核,切掉Apln-CrexER的rox-ER-rox,使得Apln-CrexER变成持续表达的Apln-Cre,而一旦表达Apln的细胞中的Cx40基因启动,那么Apln-Cre的Cre就会入核,切掉Cx40-LSL-GFP的loxP-stop-loxP,使得该细胞亮绿色,也就是表达过Apln的毛细血管衍变成动脉(表达Cx40)后就会被绿色标记(图A)。该系统通过将Apln-CrexER变成Apln-Cre,突破了Apln-CreER只能在成体心脏中标记新生毛细血管的限制,同时通过Cdh5-DreER保留了用他莫昔芬作为诱导事件发生的优势。其次,研究人员引入Cx40-LSL-GFP作为报告基因,将荧光标记限制在表达Cx40的动脉中,做到了只看毛细血管衍生的动脉,克服了标记所有毛细血管的缺陷。利用这套灵敏且清晰的系统,研究人员期望在心脏损伤过程中记录所有毛细血管动脉化产生动脉的事件。
为了检测该系统是否符合预期,研究人员基于新生期仍发生毛细血管动脉化的既有知识,对新生的Cdh5-DreER;Apln-CrexER;Cx40-LSL-GFP三基因型小鼠开展实验。研究人员对p0天的三基因小鼠注射他莫昔芬,在p2天对该小鼠进行心肌缺血(MI)手术,p6天收取该小鼠的心脏进行分析(图B)。全组织荧光照片的结果表明,MI 后形成了清晰的GFP+侧支动脉,MI组的动脉数量较未损伤组要多,且通过免疫荧光染色共染平滑肌的标志物aSMA与GFP, 证实GFP阳性的细胞都被aSMA包裹,表明毛细血管动脉化形成了侧支动脉(图B)。以上结果既表明该系统可用于追踪毛细血管动脉化产生的新动脉,也揭示了在新生期心脏损伤修复过程中的毛细血管内皮细胞贡献给侧支动脉的重要生物学过程。
为了在成体损伤情况下探究毛细血管动脉化产生动脉的情况,研究人员对8周大的Cdh5-DreER;Apln-CrexER;Cx40-LSL-GFP三基因型小鼠进行他莫昔芬注射,为避免他莫昔芬残留对实验结果的影响,研究人员在他莫昔芬注射后两周才对小鼠进行心梗手术(图C)。为探究不同心梗类型下毛细血管的动脉化,研究人员引入了三种心梗模型,包括主动脉弓缩窄手术(TAC),心肌缺血再灌注(MI/R)和心肌缺血(MI)。全组织荧光照片的结果显示,在TAC和MI/R心梗模型下几乎看不到GFP阳性的信号,而MI后可看到明显的GFP阳性的血管形态(图C)。为了更加精细地探究该GFP阳性的细胞是否是动脉内皮细胞,研究人员对三种心梗模型中收到的心脏组织分别进行切片染色,利用免疫荧光染色的实验技术,将GFP与aSMA、SM22、SM-MHC三种平滑肌细胞的标志物共染。结果表明,MI后出现的GFP阳性的细胞确实被aSMA、SM22、SM-MHC阳性的平滑肌细胞包裹,证实该由毛细血管衍生而来的GFP阳性的细胞是动脉内皮细胞(图D)。此外,对TAC和MI/R模型下得到的心脏样本进行连续切片,均没有检测到GFP信号,为排除该系统在这两种模型下效率较低的可能,研究人员引入了R26-LSL-tdTomato的小鼠,对Cdh5-DreER;Apln-CrexER;Cx40-LSL-GFP;R26-LSL-tdTomato进行TAC或者MI/R,收取其心脏样本进行切片染色,发现大量的tdTomato信号(图E),该结果表明,在TAC和MI/R模型下,Cdh5-DreER可以高效率切除Apln-CrexER的rox-ER-rox,使得Apln-Cre得以进一步切除R26-LSL-tdTomato的loxP-stop-loxP, 从而将毛细血管内皮细胞标记成tdTomato。因此,研究人员推断,TAC或者MI/R心梗模型下没有检测到GFP阳性的动脉内皮细胞,不是由于系统效率的原因,而是在这两种损伤模型下,心脏的缺血程度不足以刺激毛细血管动脉化的发生。换言之,在严重的MI心梗模型下,存在毛细血管动脉化产生新的冠状动脉。
综上,周斌组研究人员基于实验室建立的双同源重组酶介导的谱系示踪技术,开发出一套更加灵敏且清晰的系统,实现了在成体损伤条件下追踪毛细血管动脉化产生动脉的目标。这项研究结果丰富了成体损伤条件下新生动脉来源的知识,为心脏损伤后血管修复与再生治疗提供了新思路。
分子细胞卓越中心博士研究生韩茂莹和刘子鑫为该论文的共同第一作者,周斌研究员为该论文通讯作者。该工作也得到了复旦大学附属中山医院颜彦教授和香港中文大学Kathy O. Lui教授的大力支持。感谢分子细胞卓越中心动物平台和细胞分析技术平台对本研究的大力支持,感谢中科院、基金委、科技部以及上海市科委等部门的经费支持。
文章链接:https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.121.056249